Reportage und Interview über Seltene Erkrankungen, März 2023
Ich möchte Lebensqualität und Teilhabe für meine Kinder
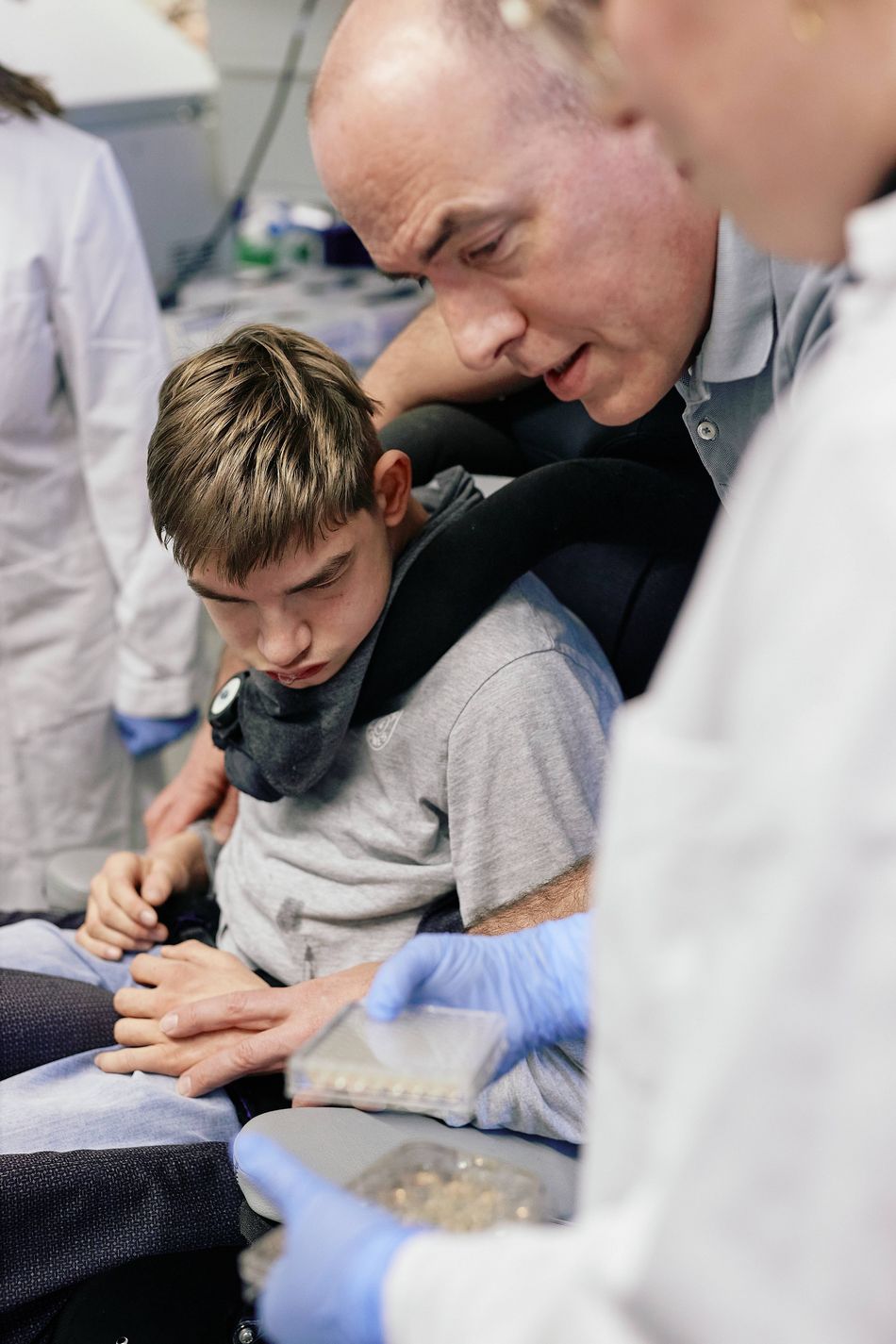
Die Brüder Jonas (18) und Felix (16) sind beide an der seltenen neurologischen Erbkrankheit PCH-2 erkrankt und mehrfach schwerstbehindert. Ihr Vater Axel Lankenau (49) und ein Pflegeteam kümmern sich rund um die Uhr um die Jungs. Um die Erkrankung besser zu verstehen, hat das Hertie-Institut für klinische Hirnforschung (HIH) in Tübingen nun mit Kollaborationspartnern an den Unikliniken Tübingen und Freiburg und dem Verein PCH-Familie e.V. eine Studie gestartet, die von der Chan Zuckerberg Initiative mit zwei Millionen US-Dollar gefördert wird. Auch Felix nimmt daran teil. Wie die Familie das Leben mit der Krankheit meistert und die Forschenden mit ins Boot holt, lesen Sie hier.
Das Glück liegt in den kleinen Dingen, heißt es. Das Lachen eines Kindes, ein Ausflug an den See oder einfach ein weiterer Tag gemeinsame Wohlfühl-Zeit. Für Axel Lankenau aus Böblingen gibt es viele dieser Momente, so sagt er, er würde sie regelrecht „aufsaugen und bewusst herbeiführen“. „Diese schönen Erlebnisse sind für mich Glück und Teil meiner Bewältigungsstrategie“, so der promovierte Informatiker. „Sie geben mir Kraft und laden meinen Akku auf, so dass ich in schwierigen Zeiten immer wieder davon zehren kann.“
Jonas (18) und Felix (16), die Söhne von Axel Lankenau, sind von einer sehr seltenen Erbkrankheit betroffen und beide mehrfach schwerstbehindert. Sie können nicht gehen und nicht sprechen, und weil ihnen das Schlucken so schwerfällt, könnten sie in einem unbeobachteten Moment ersticken. Rund um die Uhr kümmern sich ihr alleinstehender Vater und ein Team von 15 Pflegefachkräften in drei Schichten um die Brüder. Ihre Krankheit nennt sich pontozerebelläre Hypoplasie Typ 2 (PCH-2) und wird durch einen Gendefekt ausgelöst, der von beiden Elternteilen übertragen werden muss, und der zu schweren Entwicklungsstörungen führt. Nicht einmal 100 Menschen in Deutschland sind von der bisher unheilbaren Krankheit betroffen, und auch die Lankenaus wussten lange Zeit nicht, was die Diagnose für ihren erstgeborenen Sohn bedeuten würde:
„Jonas war von Anfang an auffällig, konnte schlecht trinken, schlucken und fixieren, dann fiel er beim Kinderarzt durch die U4-Untersuchung, und wir sollten mit ihm ein MRT machen lassen“, so der Vater. „Als dann die PCH-2-Diagnose kam, sagte man uns, dass Jonas´ Koordinationsfähigkeit ein Leben lang beeinträchtigt sein würde.“ Also kein Klavierspielen? Kein Fahrradfahren wegen der Balance? Das waren „die schlimmsten“ Befürchtungen, die der Vater damals hatte, und muss heute fast darüber schmunzeln. „Es wird irgendwo dazwischen liegen“, sagte die Ärztin - und entließ die Eltern in einen Irrtum, der mit jedem Tag größer wurde. Erst durch eine Studie, die sie im Internet gefunden hatten, erfuhren sie, dass Kinder mit PCH-2 niemals werden sprechen, laufen oder aufrecht stehen können. Und: Die Hälfte der 16 Jungen und Mädchen, die an der Studie teilgenommen hatten, war im Grundschulalter verstorben.
Lebensqualität für die Kinder
„Wir haben uns lange Zeit bemüht, den Ärzten eine Fehldiagnose nachzuweisen“, sagt Axel Lankenau, der damals noch bei einem großen Unternehmen angestellt war, „akribisch hatten wir aufgezeichnet, was Jonas alles gelernt hat, zum Beispiel das Fixieren.“ Bis ein Arzt in Tübingen die Eltern mit einem Schlag von ihrem „Verdrängungsgipfel“ geholt habe: „Das MRT ist eindeutig: Jonas wird nie ein eigenständiges Leben führen können.“
Noch heute klingen dem Vater die Worte im Ohr. Doch der erfahrene Mediziner war ein kluger Mann und gab den Eltern einen Rat, den Axel Lankenau bis heute nicht vergessen hat: Jedes Kind habe eine Art Entwicklungsrahmen, und die Größe sei für jedes Kind unterschiedlich groß, je nach Lebensumständen und genetischer Disposition, so der Arzt. Der Rahmen von Jonas sei sicher viel kleiner als der von einem gesunden Kind, aber er wäre nicht Null. Die Aufgabe der Eltern könne es sein, Jonas ein möglichst gutes Leben innerhalb seines Rahmens zu bieten. „Für mich ist das seitdem mein Arbeitsauftrag“, sagt Axel Lankenau, der sich seit der Trennung von seiner Frau vor fünf Jahren zuhause allein um seine Jungs kümmert. „Ich möchte Lebensqualität und Teilhabe für meine Kinder.“
Dass auch der zweite Sohn Felix das defekte Gen in sich tragen würde, war für das Ehepaar Lankenau damals noch nicht abzusehen, es gab den Nachweis darüber noch nicht. Die Schwangerschaft verlief problemlos, und Felix, der 2007 zur Welt kam, verhielt sich unauffällig. „Er trank wie ein Weltmeister, saß entspannt im Maxi-Cosi und konnte seine Umwelt fixieren. Ganz anders als Jonas. Wir bekamen sogar schriftlich, dass Felix völlig gesund sei“, so der Vater. Gut fünf Monate blieb die Unbeschwertheit in der kleinen Familie, bis die Tage zunahmen, an denen sich Felix plötzlich nicht mehr im Unterarmstütz halten konnte, seine Augen das Spielzeug aus dem Blick verloren, das Schlucken schwer fiel - und das MRT auch für ihn die Diagnose ausspuckte: PCH-2.
„Von einem Moment auf den nächsten brach die ganze Hoffnung auf ein gesundes Geschwisterkind weg“, sagt Axel Lankenau, „das war ein sehr viel schlimmerer Nackenschlag als bei Jonas, weil die Dimensionen einfach größer waren.“ Wie das nur aushalten? Viele Tränen, Gespräche, aber auch stumme Momente waren nötig, um sich einigermaßen wieder zurechtzufinden. Und am Ende habe auch diese Krise etwas Gutes gehabt, sagt Axel Lankenau: „Wir waren so fertig und überfordert, dass wir bereit waren, Hilfe anzunehmen. Bisher hatten wir Jonas allein gepflegt, die vielen schlaflosen Nächte hingenommen, aber nun war klar, dass wir das mit zwei schwerstbehinderten Kindern nicht packen würden.“

Hoffnung auf neue Therapien
Die Eltern ließen sich im Kinderhospiz im Allgäu beraten, vernetzten sich mit anderen Betroffenen, stellten ein eigenes Pflegeteam ein. Axel Lankenau hat seinen IT-Job gekündigt, ist nun selbstständiger Berater für Familien mit behinderten Kindern. Und er engagiert sich in dem Elternverein „PCH-Familie“, auf dessen Initiative gemeinsam mit Neurobiologen und Medizinern das Verbundprojekt „PCH2cure“ gegründet wurde, um die Lebensqualität der Betroffenen zu verbessern. Denn noch immer quälen starke Unruhe, Reizbarkeit, aber auch unklare Schmerzen und Probleme mit dem Verdauungstrakt die Erkrankten. „Wir hoffen sehr, dass durch dieses Projekt neue Therapiemöglichkeiten entdeckt werden, die unseren Kindern helfen können“, sagt Axel Lankenau. Das Hertie-Institut für klinische Hirnforschung in Tübingen hat gerade unter Leitung von Biologin Dr. Simone Mayer eine Studie gestartet, um die PCH-2 besser zu verstehen (siehe Interview am Ende des Textes). Auch Felix trägt als Studienteilnehmer dazu bei, der Krankheit auf die Schliche zu kommen. Im nächsten Jahr soll es mit 20 PCH-Kindern, ihren Familien und dem „PCH2cure“-Team eine Woche auf Ostseekreuzfahrt gehen, „damit die Ärzte und Wissenschaftler die Möglichkeit haben, möglichst viele betroffene Kinder live zu erleben und zu beobachten“, sagt Axel Lankenau.
Heute verbringen die Brüder ihre Tage nach einem festen Rhythmus: Am Vormittag besuchen sie die Berufsschulstufe einer Schule in Stuttgart, lernen dort, was Mobilität in der Stadt bedeutet, aber auch, wie man einen Alltag lebt. Am Nachmittag gibt es mal Ergo-, Physio- und Musiktherapie, und am Wochenende geht’s mit Papa und jemandem aus dem Pflegeteam raus in die Natur. Aber Jonas und Felix haben auch Freunde, die sie besuchen, und die sie nicht vergessen haben. Dann steuern sie mithilfe einer besonderen Software durch die Augenbewegungen Spiele auf ihrem Tablet, hören Musik oder gucken Filme - wohl wie andere Jungs auch in diesem Alter.
Wie es weitergeht? „Ich habe gelernt, mit der Situation umzugehen“, sagt Axel Lankenau, „und ich habe Unterstützung, vor allem, wenn es den Jungs schlecht geht. Ich hangle mich von Jahr zu Jahr, und freue mich, wenn ich meinen Söhnen möglichst lange ein selbstbestimmtes und schönes Leben bereiten kann.“ Zum Beispiel mit Ausflügen, wie im vergangenen Sommer die Segeltour auf dem Ijsselmeer. Oder der Vatertag am Rheinfall in Schaffhausen.
Für die Osterferien hat Axel Lankenau einen Urlaub in der Schweiz geplant. Mit Skilaufmöglichkeit für Rollstuhlfahrer. Freunde kommen auch mit. „Darauf freue ich mich sehr.“ Dann wird Axel Lankenau wieder glückliche Momente „aufsaugen“ und sie ganz tief in seinem Herzen abspeichern. Für jetzt - und für alles, was kommt.
INFO Text von Rena Beeg für die Gemeinnützige Hertie-Stiftung

Neue Studie zu seltener neurologischer Erbkrankheit PCH-2 am Start
3 Fragen an Dr. Simone Mayer, Forschungsgruppenleiterin Molekulare Hirnentwicklung am Hertie-Institut für klinische Hirnforschung (HIH) in Tübingen.
1. Sie leiten eine Studie zu einer extrem seltenen Erbkrankheit, worum geht es dabei?
Die pontozerebelläre Hypoplasie ist eine seltene schwere neurologische Erkrankung, die in mehrere Subtypen eingeteilt wird. Wir beschäftigen uns mit dem Typ 2 (PCH-2), der am weitesten verbreitet ist. In Deutschland liegt die Zahl der Betroffenen unter 100. Die Betroffenen haben schwerste Entwicklungsstörungen und eine eingeschränkte Lebenserwartung. Ursache ist ein Gendefekt, der dazu führt, dass das Kleinhirn und der Hirnstamm extrem verschmächtigt sind. Damit die Erkrankung ausbricht, müssen beide Elternteile Träger des defekten Gens sein. Um den Verlauf der Krankheit und die zugrundeliegenden Mechanismen besser zu verstehen, mit dem Ziel eine Therapie zu entwickeln, haben wir uns auf Initiative des Elternvereins „PCH-Familie e.V.“ 2019 als „PCH2cure“ Konsortium mit Kinderärzten der Unikliniken Tübingen und Freiburg zusammengeschlossen. Wir freuen uns sehr, dass „PCH2cure“ jetzt mit zwei Millionen US-Dollar von der Chan Zuckerberg Initiative gefördert wird, wovon 400.000 Dollar direkt an den Elternverein gehen. Im wissenschaftlichen Teil der Studie, den ich leite, wollen wir die Krankheitsmechanismen mit einem interdisziplinären Ansatz untersuchen, der sowohl einen Fokus auf der genaueren Analyse der Neurodegeneration mittels Bildgebung bei Patienten beinhaltet als auch die Untersuchung von Darmgewebe und neuronaler Zellkulturmodelle. Im Teil der Studie, den ich in meiner Arbeitsgruppe am HIH bearbeite, wollen wir nun in der Petrischale herausfinden, warum das betroffene Gen, das wir eigentlich in jeder Zelle zur Eiweißherstellung brauchen, in gewissen Hirnregionen und auch zu gewissen Zeiträumen der Entwicklung einen so spezifischen Effekt haben kann, also eine PCH-2 auslöst. Diese Frage ist komplett ungeklärt, stellt aber einen Schlüssel für mögliche Therapieansätze dar.
Das Hertie-Institut für klinische Hirnforschung (HIH) in Tübingen ist eines der bundesweit größten und modernsten Zentren zur Erforschung neurologischer Erkrankungen. Das HIH ist ein modellhaftes Forschungszentrum im Zusammenspiel öffentlicher Ressourcen und privater Stiftungsmittel: Es wurde 2001 von der Gemeinnützigen Hertie-Stiftung, dem Land Baden-Württemberg, der Eberhard Karls Universität Tübingen, ihrer medizinischen Fakultät sowie dem Universitätsklinikum Tübingen gegründet und 2004 eröffnet.
2. Warum ist der enge Austausch zwischen Forschenden und Betroffenen so wichtig?
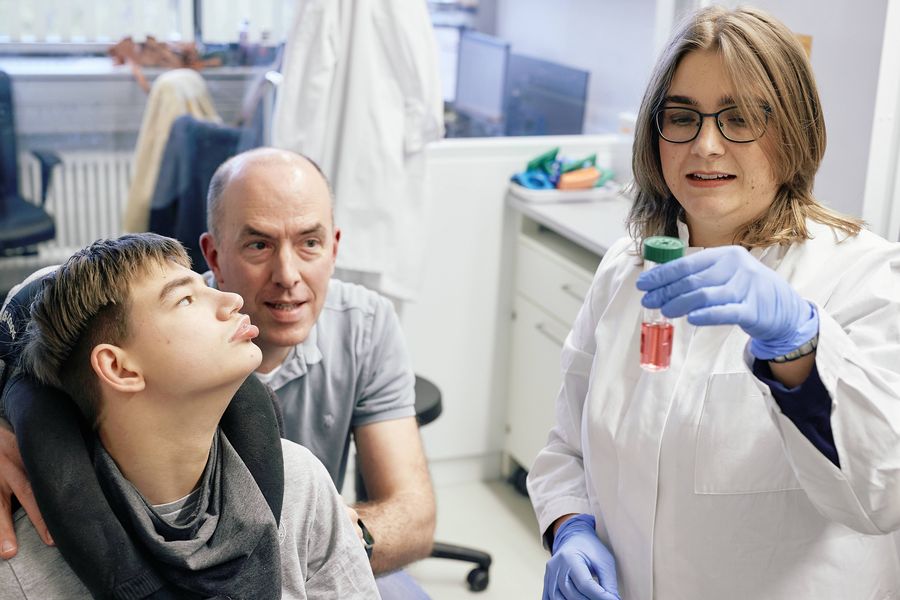
Dass wir mit „PCH2cure“ extra ein Verbundprojekt gegründet haben, ist in dieser Form neu und könnte durchaus als Modell für andere Forschungsprojekte dienen. Die enge und standortübergreifende Zusammenarbeit zwischen Biologen, Medizinern und den Familien spielt eine Schlüsselrolle, um die Perspektive für die Erkrankten zu verbessern. Für mich als Biologin, die meistens am Schreibtisch oder im Labor sitzt, bekommt die Erkrankung jetzt ein Gesicht. Als uns die Brüder Lankenau (siehe Haupttext) im Labor besuchten, war das sehr beeindruckend für mich. Mir wurde noch einmal sehr klar, wie wichtig unsere Forschung ist, um neue Therapien entwickeln zu können, oder die Erkrankung irgendwann ganz zu verhindern. Mein Team und mich motiviert das sehr.
3. Für Ihre Forschung nutzen Sie sogenannte Hirnorganoide. Was ist das genau?
Hirnorganoide sind dreidimensionale Zellkulturen, die dem natürlichen menschlichen Hirngewebe sehr ähneln. Sie werden mithilfe von Stammzellen entwickelt, die wir zuvor aus Hautzellen von PCH-2-Patienten gewonnen haben. Die Organoide bieten die Chance, Krankheitsmechanismen in der Petrischale zu modellieren, in sie einzugreifen und sie dadurch besser zu verstehen. Die medizinische Grundlagenforschung hat in den vergangenen Jahren mithilfe von Organoiden enorme Fortschritte erzielt. Darauf bauen wir auf.
INFO Interview von Rena Beeg für die Gemeinnützige Hertie-Stiftung



